厦门大学陈鹭剑、胡学佳与武汉大学杨奕课题组:3D打印器件辅助的声学细胞三维组装
发布日期:2022-08-11
浏览量:1508次

在前沿的组织工程、药物开发、甚至临床应用中,模拟体内组织结构和环境的体外模型构建都是十分重要的条件,而细胞或微结构单元的组装方式以及细胞外基质环境在组织功能化过程中扮演关键角色,这也就促使了三维组织结构打印技术的发展。在这些技术中,以投影式光固化、挤出式打印技术等为代表,使用包含有细胞的水凝胶作为生物墨水材料,展现了优越的生物组织构建的能力。但是,这种打印仍局限于对生物墨水整体打印,而其中的细胞是随机分布的,难以主动的对细胞组建微结构单元,这也是目前生物打印面临的一个挑战。
近些年,声波作为一种易于集成、高生物亲和性且高精度的控制手段,在细胞的灵活操控和高效组装应用中得到广泛研究,比如将声波与微流控相结合的声流控与声镊技术,特别适合操控细胞构建类组织的体外模型。而如何将二维的声场操控技术拓展到三维,并进行三维组织结构的组装,是其迈向生物3D打印需要解决的难题。近日,厦门大学陈鹭剑教授、胡学佳助理教授与武汉大学杨奕教授课题组合作提出了一种新的解决方案:结合层片打印和声学操控细胞三维结构组装,并以题为:Smart acoustic 3D cell construct assembly with high-resolution发表于Biofabrication 期刊上。
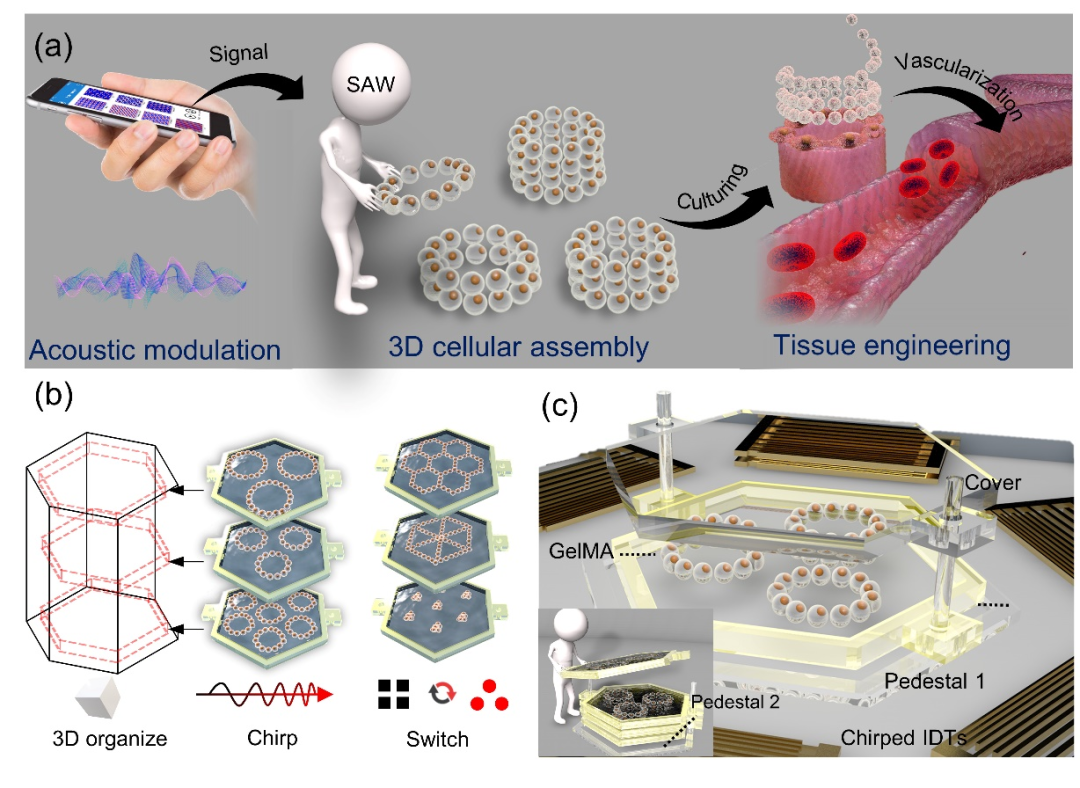
图1.声学3D细胞组装示意图。
借鉴多层光固化打印的思路,本研究提出基于声表面波在凝胶层片中直接操控细胞组成特征结构,并对层片单元进行多层组装,成功实现了细胞的三维结构组装和仿生组织构建。图一中展示了该策略的示意图,该技术在Z-切铌酸锂基底上设计具有六重旋转对称的换能器配置,保证较大的调制自由度,通过波矢组合、相位组合以及振幅调制(图1b),能够将层片中细胞组装成为多样的结构。而为了将表面波产生的二维声场和二维细胞结构拓展到三维空间,使用了摩方精密的PμSL高精度光固化3D打印技术(nanoArch P150超高精度光固化3D打印系统),来制造高精度模块化框架,与表面波声场耦合,并在该框架中实现细胞组装(图1c)。GelMA 60作为生物墨水,经过光固化后,可形成具有微观结构的凝胶层片。再将该凝胶层片作为二维单元,进行多层的对齐组装以及使用水凝胶融合,即可得到被凝胶基质固定的微观三维结构。

图2.结合3D打印模组的器件示意图。
作为论证,图三展示结合3D打印组件的声波装置调制产生的多种声场结构,其具有不同的特征单元,比如类血管的环形结构、类肝小叶的蜂巢结构以及密堆的点阵结构等等,并且通过实验验证其进行灵活细胞组装的能力(图3b)。通过二次三维组装,研究人员实现了多种三维的细胞尺度的类组织模型构建,包括空心管状的毛细血管组织、交织的组织结构以及类肝小叶蜂巢组织等(图4)。这些特征单元的尺度取决于声场的周期,可以通过设计实现在几十微米到数百微米变化。而在三维空间上,由于使用高精度打印的单元结构,这些层片的厚度可以低至100微米,能够通过设计不同层间距离适配不同组织高度的需求。并且这些三维类组织模型经过培养展现了较好的活性,微观上紧密连接的仿生结构进一步促进了细胞与组织功能化的过程,比如实验中验证发现,管状的三维模型在长期培养的过程中细胞之间相互连接融合并展现血管化趋势。
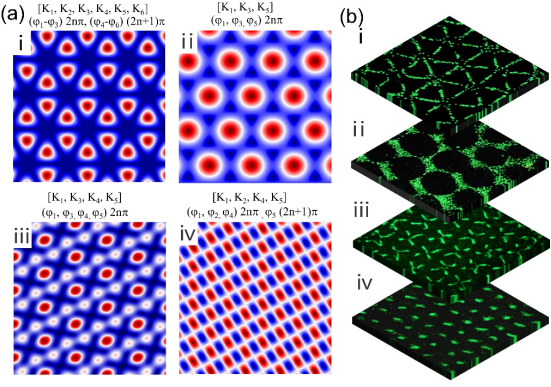
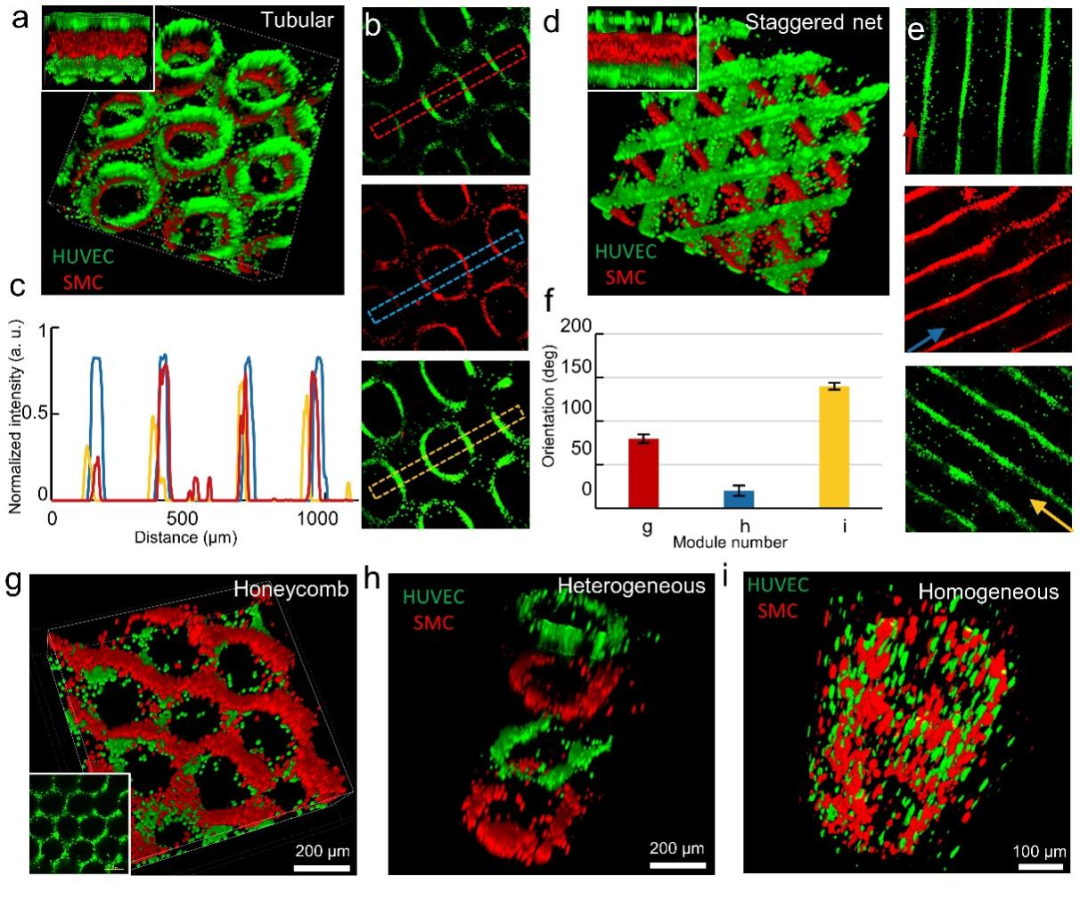
图4.对细胞层片单元进行多层组装,构建的多种三维结构荧光共聚焦图。
该声学细胞3D组装技术将声表面波的二维操控能力拓展到三维空间,展现了独特的优势,比如直接对细胞组装、精准构造组织结构、灵活可控以及操作简便。这项研究展现了对生物墨水打印之外对微观介质构建的能力,从新的维度提出了一种创新的技术路线。
论文信息:Hu, X. J.; Zheng, J. J.; Hu, Q. H.; Liang, L.; Yang, D. Y.; Cheng, Y. X.; Li, S. S.; Chen, L. J.; Yang, Y., Smart acoustic 3D cell construct assembly with high-resolution. Biofabrication 2022, 14 (4),045003
DOI:https://doi.org/10.1088/1758-5090/ac7c90