精准的肿瘤诊疗技术是改善患者预后、降低复发风险的关键。然而,传统微创介入导管在临床应用中仍面临诸多挑战:导航灵活性不足、功能单一、依赖反复X射线成像,且难以在术中实时获取肿瘤边界信息。现有的磁控导管虽在外场驱动下展现出优异的导航能力,但受限于制造工艺,往往难以在微型化尺度内集成传感、给药、治疗等多种功能。因此,开发一款集高精度导航、实时诊断与精准治疗于一体的多功能微创器械,对于提升肿瘤介入诊疗水平具有重要意义。
三维(3D)多轴打印技术为多功能医疗器械的集成化与微型化开辟了新路径。近期,中山大学蒋乐伦教授与谢曦教授团队在《Nature Communications》上发表题为“Magnetic-driven Multifunctional Optoelectronic Catheter for in vivo chemical mapping and precisely guided-tumor therapy”的研究论文。该研究开发了一款直径为2.5 mm的磁性驱动多功能光电导管(MDMOC),集成了磁控导航、多参数电化学传感、药物靶向递送以及局部光动力治疗等多项功能,为实现复杂肿瘤的精准诊疗提供了一体化平台(图1)。
在系统设计上,研究者通过自研的多芯同轴3D打印技术,一步法打印了集成液态金属导电通道的多轴柔性鞘管。液态金属使导管弯曲柔性大幅提升,同时确保多通道电信号稳定传输。导管表面通过紫外光交联形成水凝胶涂层,显著降低摩擦系数,改善了导管在复杂解剖环境中的通过性。内置磁环不仅赋予导管优异的磁响应变形能力,还使其在X射线成像下清晰可视。值得注意的是,作者通过摩方精密面投影微立体光刻(PμSL)3D打印技术(nanoArch® S140,精度:10 μm)制作了前端电化学传感阵列保护外壳结构。该箭簇状外壳不仅对内部传感器的有效保护,其内部菱形孔的设计还能保证待测组织液顺利流通。
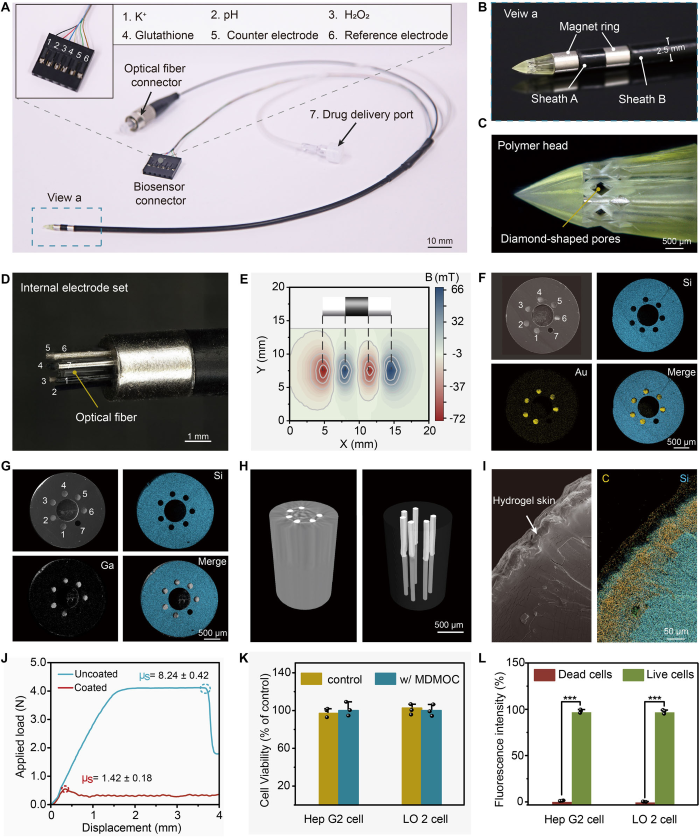
图1. MDMOC的实物图与结构表征。
为了验证MDMOC的肿瘤边界识别能力,研究团队在兔原位肝癌模型中进行了多点原位化学检测。导管内置的四种电化学传感器分别针对肿瘤微环境四种标志物——pH、过氧化氢(H₂O₂)、钾离子(K⁺)和谷胱甘肽(GSH)。通过在肿瘤及周边组织进行多点检测,研究者绘制了四种标志物的浓度分布热图,清晰呈现肿瘤-正常组织界面的浓度梯度。多模态数据融合显著提升了边界检测精度,实现了接近病理学金标准的肿瘤勾勒效果。
进一步,研究者在小鼠原位肝癌模型中验证了MDMOC的诊疗一体化性能。通过导管内置通道局部注射光敏剂,并联合光纤传导激光进行原位光动力治疗。与全身给药相比,局部递送显著增加肿瘤内药物蓄积。治疗后监测显示,MDMOC组肿瘤生长抑制效果显著,同时主要器官未观察到明显损伤,证实了其高效低毒的治疗优势。
在巴马猪模型中,研究者评估了MDMOC的临床适用性。在数字减影血管造影引导下,MDMOC在外磁场驱动下成功穿越复杂血管路径,精准进入目标血管分支并完成对比剂注射。在腹腔镜辅助下,MDMOC实现了对肝脏表面多病灶的定位穿刺、原位电化学检测和模拟给药,并在心脏搏动导致的肝脏位移中保持稳定贴靠。
总结:研究者开发的MDMOC技术为肿瘤微创介入诊疗提供了一个功能高度集成的多功能平台。通过磁控导航、多模态原位传感与局域治疗的协同整合,MDMOC能够在复杂体内环境中实现快速“感知-决策-治疗”闭环,不仅实现了肿瘤边界的精准化学描绘,还显著提升了治疗的针对性与安全性。未来,该技术有望拓展至更广泛的肿瘤类型和介入场景,推动个性化精准肿瘤治疗的发展。
原文链接:https://doi.org/10.1038/s41467-026-70529-6